Οξεοβασικές Διαταραχές σε ουρητηρο-εντεροστομίες
(Σιγμο- και εντερο-στομίες) και σε μεταμόσχευση παγκρέατος
Ιωάννης Γ. Γριβέας
Διευθυντής Μονάδας Τεχνητού Νεφρού 401ΓΣΝΑ
Κύρια σημεία
- Ιστορικά η πρώτη προσπάθεια εκτροπής της πορείας των ούρων έγινε με τη δημιουργία μίας οδού επικοινωνίας μεταξύ του εντέρου και των ουρητήρων. Σε αυτές τις πρώτες χειρουργικές πρακτικές χρησιμοποιήθηκε ο πρωκτός ως μηχανισμός εγκράτειας των ούρων. Η εμφάνιση ουρητηρικών στενώσεων, η δημιουργία λίθων, τα συχνά επεισόδια λοιμώξεων με συνοδό σήψη και περιτονίτιδα οδήγησαν σε υψηλά ποσοστά θνητότητας. Σε κλινικό επίπεδο η ακράτεια έγινε συχνό φαινόμενο.
- Η βελτίωση των χειρουργικών τεχνικών και η πιο ολοκληρωμένη υποστηρικτική φροντίδα (καλύτερα αντιβιοτικά, σωστότερη χρήση των υγρών, κ.α.) έχουν αυξήσει το προσδόκιμο της ζωής ασθενών με κάποιας μορφής ουρητηρο-εντερο-στομία και διευρύνει το εύρος των εφαρμογών της σε όλες τις ηλικίες των ασθενών.
- Η εκτροπή κατά Bricker (ileocutaneostomy) είναι σήμερα το πιο συχνά χρησιμοποιούμενο είδος εκτροπής σε όλο τον κόσμο.
- Η κύρια διαταραχή που εμφανίζεται όταν ειλεός ή κόλον χρησιμοποιείται για την στομία είναι υπερχλωραιμική μεταβολική οξέωση.
- Η θεραπεία της υπερχλωραιμκής μεταβολικής οξέωσης περιλαμβάνει χορήγηση αλκαλιωτικών παραγόντων και/ή αναστολέων της μεταφοράς Cl-. Η χορήγηση από του στόματος διττανθρακικών μπορεί να αναπληρώσει το έλλειμμα στην οξεοβασική ισορροπία, από κάποιους ασθενείς όμως δεν γίνεται εύκολα ανεκτή.
- Οι ασθενείς με εκτροπή των ούρων παρουσιάζουν ελαττωμένες αποθήκες καλίου λόγω εντερικών απωλειών, ωσμωτικής διούρησης και νεφρικής έκκρισης. Πιο έντονο είναι το φαινόμενο στους ασθενείς με ουρητηροσιγμοειδοστομία.
- Κλινικά σημαντική υπασβεστιαιμία δεν είναι συχνή. Συμπληρώματα ασβεστίου είναι η θεραπεία εκλογής. Η υπομαγνησιαιμία είναι μια σπάνια κατάσταση μετά από ουρητηρο-εντερο στομία.
- Μετά από 20 χρόνια παρακολούθησης, έως και 20% των ασθενών με ουρητηρο-εντερο στομία θα έχουν νεφρολιθίαση. Στην τακτική παρακολούθηση των ασθενών με εκτροπή των ούρων, πρέπει να περιλαμβάνεται η υπερηχογραφική απεικόνιση των νεφρών για τον έλεγχο σχηματισμού λίθων.
- Στην κλινική πράξη, σε σειρές ασθενών με ουρητηρο-εντερο-στομίες σοβαρές μεταβολικές διαταραχές των οστών που να έχουν οδηγήσει σε οστεομαλακία δεν έχουν παρατηρηθεί. Το πιό πιθανό είναι να παρατηρηθούν μικρές διαταραχές της αφαλάτωσης των οστών στην πλειοψηφία των ασθενών που έχουν ουρητηρο-εντερο-στομίες για μέγαλη χρονική περίοδο.
- Το βασικό αίτιο των μεταβολικών διαταραχών στους ασθενείς μετά από μεταμόσχευση παγκρέατος είναι η απώλεια μεγάλων ποσοτήτων παγκρεατικού υγρού πλούσιου σε αλκαλικά ένζυμα μέσω της ουροφόρου οδού. Μεταβολική οξέωση, υπονατριαιμία και απώλεια υγρών από τον εξωκυττάριο χώρο μπορεί να παρατηρηθούν.
Εισαγωγή
Στην ουρολογική πρακτική υπάρχουν μία σειρά από κλινικές οντότητες που οδηγούν σε σοβαρά προβλήματα του κατώτερου ουροποιητικού συστήματος. Το έντερο έχει χρησιμοποιηθεί ως αντικαταστάτης ουρητήρα ή/και ουροδόχου κύστης σε πολλές των περιπτώσεων.
Ιστορικά η πρώτη προσπάθεια εκτροπής της πορείας των ούρων έγινε με τη δημιουργία μίας οδού επικοινωνίας μεταξύ του εντέρου και των ουρητήρων. Σε αυτές τις πρώτες χειρουργικές πρακτικές χρησιμοποιήθηκε ο πρωκτός ως μηχανισμός εγκράτειας των ούρων. Η εμφάνιση ουρητηρικών στενώσεων, η δημιουργία λίθων, τα συχνά επεισόδια λοιμώξεων με συνοδό σήψη και περιτονίτιδα οδήγησαν σε υψηλά ποσοστά θνητότητας. Σε κλινικό επίπεδο η ακράτεια έγινε συχνό φαινόμενο. Ο βασικότερος λόγος για όλα τα παραπάνω προβλήματα είναι ότι το έντερο δεν είναι «φτιαγμένο» για να αποτελεί τμήμα της ουροφόρου οδού. Η βελτίωση των χειρουργικών τεχνικών και η πιο ολοκληρωμένη υποστηρικτική φροντίδα (καλύτερα αντιβιοτικά, σωστότερη χρήση των υγρών, κ.α.) έχουν αυξήσει το προσδόκιμο της ζωής ασθενών με κάποιας μορφής ουρητηρο-εντερο-στομία και διευρύνει το εύρος των εφαρμογών της σε όλες τις ηλικίες των ασθενών. Στην πράξη, με την μακρύτερη πορεία των ασθενών αυτών οι κλινικοί ιατροί καλούνται να αντιμετωπίσουν εμφανή και σοβαρά μεταβολικά προβλήματα, τα οποία μπορούν να επηρεάσουν την ποιότητα ζωής. Το τμήμα του εντέρου που συνδέεται με την ουροφόρο οδό έχει ρόλο στο είδος των μεταβολικών διαταραχών που προκαλούνται στον οργανισμό τόσο από την άποψη της νέας «ανατομίας» και «φυσιολογίας» της ουροφόρου οδού όσο και από την άποψη του τμήματος του εντέρου που αφαιρέθηκε από την γαστρεντερική οδό. Κατά πλειοψηφία χρησιμοποιείται τμήμα του τελικού ειλεού ή τμήματα του κόλου του εντέρου. Ο λόγος για τον οποίον προτιμώνται αυτά τα τμήματα του εντέρου είναι η καλή τους κινητικότητα, με σχετικά μακριά και άθικτα αγγεία, το τυφλό σπάνια έχει εκκολπώματα, η πιο προσιτή χειρουργική τεχνική για την αναστόμωση και τέλος η χρήση της ειλεοτυφλικής βαλβίδας ως μηχανισμού εγκράτειας. Ωστόσο δεν υπάρχει «απόδειξη» ότι τα τμήματα αυτά του εντέρου υπερτερούν των άλλων.
Η φύση και ο βαθμός των μεταβολικών διαταραχών που εμφανίζονται εξαρτώνται πρωτίστως από τον βαθμό ανταλλαγής ιόντων και αλάτων κατά μήκος του τμήματος του εντέρου που χρησιμοποιήθηκε. Τα χαρακτηριστικά της ανταλλαγής αυτής επηρεάζονται από την διάρκεια της επαφής των ούρων με το έντερο, από το τμήμα, την επιφάνεια και το μήκος του εντέρου που χρησιμοποιήθηκε, την συγκέντρωση τους στα ούρα, το p H και την ωσμωτικότητα των υγρών. Οι οποιεσδήποτε διαταραχές εμφανίζονται αμέσως με την δημιουργία της στομίας και συνήθως η δραστηριότητα της διαδικασίας μεταφοράς ιόντων ελαττώνεται με το χρόνο. Ωστόσο στην άμεση μετεγχειρητική περίοδο η παραμονή καθετήρων ή/και των stents στην αναστόμωση περιορίζει την χρονική επαφή των ούρων με τον εντερικό βλενογόννο. Από την στιγμή της απομάκρυνσης και του ουροκαθετήρα (περίπου την 10η μετεγχειρητική ημέρα) το μεταβολικό προφίλ αλλάζει. Αρκετές επιπλοκές γίνονται εμφανείς μήνες ή και χρόνια μετά την δημιουργία της στομίας. Εξαιτίας αυτού του λόγου η επί μακρόν σωστή παρακολούθηση κρίνεται απαραίτητη για την αποφυγή επιπλοκών ή προβλημάτων. Οι χειρισμοί στην φάση της παρακολούθησης είναι σε κάποιες περιπτώσεις υπό συζήτηση. Αυτό το πεδίο της μελέτης χαρακτηρίζεται από πληθώρα ετερόκλητων μεταβλητών (όπως η ταυτόχρονη χημειοθεραπεία, νευρογενείς ασθένειες,η ύπαρξη συγγενών ανωμαλιών, κ.λπ.). Ως εκ τούτου, οι καλές κλινικές μελέτες λείπουν και οι περισσότερες συστάσεις βασίζονται σε γνώμες εμπειρογνωμόνων με χαμηλή ποιότητα δεδομένων.
Παράλληλα με όλες τις παραπάνω μεταβολές, ιστολογικές αλλαγές επίσης παρατηρούνται στο εντερικό επιθήλιο όταν αυτό έρθει σε επαφή για μεγάλες περιόδους με ούρα. Απώλεια του ύψους των λαχνών και περιοχές ατροφίας παρατηρούνται σε τμήματα του ειλεού που έρχονται σε επαφή με ούρα. Αν αυτό επηρεάζει την ικανότητα του επιθηλιακού κυττάρου στην μεταφορά ιόντων δεν έχει εξακριβωθεί1.
Η χειρουργική προσέγγιση
Η Ουρητηροσιγμοειδοστομία ήταν η πιο διαδεδομένη τεχνική εκτροπής των ούρων μέχρι τα τέλη της δεκαετίας του 1970. Σύμφωνα με την τεχνική αυτή οι ουρητήρες αναστομώνονταν απευθείας στο σιγμοειδές και με αυτόν τον τρόπο δεν διαταρασσόταν η συνέχεια του εντέρου. Μία σειρά από προβλήματα παρουσιάζονταν στους ασθενείς με την παραπάνω θεραπευτική προσέγγιση, που ήταν ευρέως διαδεδομένη σε περιπτώσεις με εκστροφή κύστεως. Συχνά η νεφρική λειτουργία παρουσίαζε μία προοδευτική επιδείνωση με το χρόνο. Συχνά ήταν και τα φαινόμενα εμφάνισης λιθίασης, λοιμώξεων, συμφύσεων στην ουρήθρα, ενώ οι ασθενείς αντιμετωπίζονταν ως υψηλού κινδύνου για την εμφάνιση νεοπλάσματος στο κόλον (συχνότητα 10% σε περίοδο 20 ετών).
Η εκτροπή κατά Bricker (ileocutaneostomy) είναι σήμερα το πιο συχνά χρησιμοποιούμενο είδος εκτροπής σε όλο τον κόσμο. Η διαδικασία αυτή διαδόθηκε από τον Eugene M. Bricker2. Στην τεχνική αυτή, χρησιμοποιούνται 15 έως 25 εκατοστά προτελικού ειλεού (Σχ 1). Οι λόγοι για τη δημοτικότητά της τεχνικής αυτής σε σχέση με άλλους τύπους εκτροπής είναι η σχετική ευκολία και η απλότητα της διαδικασίας. Δίνει προβλέψιμα λειτουργικά αποτελέσματα. Δεν υπάρχει κανένας κίνδυνος για απρόσμενη ακράτεια, για κατακράτηση ούρων ή για προβλήματα καθετηριασμού.
Η χρήση ενός μικρού τμήματοςτου εντέρου και το γεγονός ότι το τμήμα αυτό δεν λειτουργεί ως δεξαμενή, συνεπάγεται λιγότερες μεταβολικές επιπλοκές. Παρ 'όλα αυτά, το 10% περίπου των ασθενών με ουρητηροστομία στον ειλεό θα εμφανίσουν κάποιας μορφής μεταβολική διαταραχή που θα απαιτήσει θεραπεία.
Σχήμα 1. Εμφύτευση ουρητήρα σε τμήμα του ειλεού.
Η εικόνα προέρχεται από το Ileal Neobladder and Its Variants by Georgios Gakis, Arnulf Stenzl from EUROPEAN UROLOGY SUPPLEMENTS 9 (2010) 745–753
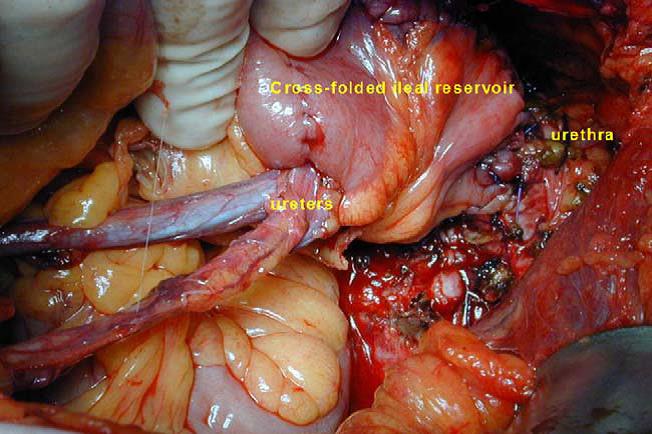
Συχνά χρησιμοποιείται το άνοιγμα του εντέρου αντίθετα από την πλευρά του μεσεντερίου προκειμένου να καταργηθούν λειτουργικές εντερικές συσπάσεις. Το W-σακκουλάκι ή σακούλα Hautmann, ο θύλακας Studer, το Ν-σακκουλάκι και η θήκη Kock είναι μερικές δημοφιλείς παραλλαγές σε αυτό.
Νεφρική Λειτουργία
Από την ηλικία των 40 ετών και μετά προοδευτικά ελαττώνεται ο ρυθμός σπειραματικής διήθησης (Glomerular Filtration Rate-GFR) με ρυθμό 1 mL/min/1,73m² από την αρχική τιμή των 100-130 mL/min/1,73m². Μετά την διενέργεια της ουρητηρο-στομίας, διάφοροι παράγοντες μπορεί να προκαλέσουν την επιδείνωση της νεφρικής λειτουργίας. Στένωση της ουρητηρο-εντερο αναστόμωσης οδηγεί σε ουρητηρική απόφραξη με επακόλουθη την νεφρική βλάβη. Υποτροποιάζουσες λοιμώξεις και λιθίαση έχουν αρνητική επίδραση στην νεφρική λειτουργία. Θεωρητικά, η ενσωμάτωση τμήματος εντέρου στην ουροφόρο οδό προκαλεί απορρόφηση μεταβολιτών από τα ούρα με αποτέλεσμα την ποικίλου βαθμού επιδείνωση της νεφρικής λειτουργίας. Ωστόσο, η ακριβής επίδραση της ουρητηρο-στομίας στην νεφρική λειτουργία δεν είναι γνωστή8. Έχει δειχθεί ότι σε αυτές τις κλινικές καταστάσεις η ελάττωση του GFR μπορεί να κινηθεί σε επίπεδα 15-25% για διάστημα 11 ετών9.
Στην κλινική πράξη, είναι σημαντικό να αναζητούνται αναστρέψιμα αίτια επιδείνωσης της νεφρικής λειτουργίας για να γίνονται οι απαραίτητες θεραπευτικές παρεμβάσεις. Είναι επίσης σημαντικό να είναι γνωστό το επίπεδο της νεφρικής λειτουργίας πριν τη διενέργεια της όποιας παρέμβασης, γιατί αυτό έχει επίδραση σε μελλοντικές αποφάσεις. Η μακροχρόνια παρακολούθηση της νεφρικής λειτουργίας, τουλάχιστον σε ετήσια βάση, κρίνεται σκόπιμη. Η κρεατινίνη ορού δεν θεωρείται από μόνη της η πιο αξιόπιστη μέθοδος εκτίμησης της νεφρικής λειτουργίας. Ο συνδυασμός της υπερηχογραφικής απεικόνισης με τη μέτρηση της κρεατινίνης ορού αποτελεί το καλύτερο screening test της νεφρικής λειτουργίας. Σε περίπτωση οποιασδήποτε αμφιβολίας ο προσδιορισμός του GFR σπινθηρογραφικά είναι το επόμενο βήμα1.
Διαταραχές της οξεοβασικής ισορροπίας
Γενικά
Η εμφάνιση οξεοβασικών και ηλεκτρολυτικών διαταραχών και η σοβαρότητα τους εξαρτάται από το τμήμα του εντέρου που χρησιμοποιείται για την διενέργεια της ουρητηροστομίας. Για παράδειγμα αν χρησιμοποιηθεί στομάχι παρουσιάζεται υποκαλιαιμική, υποχλωραιμική μεταβολική αλκάλωση. Από την άλλη αν χρησιμοποιηθεί λεπτό έντερο υπονατριαιμική, υποχλωραιμική, υπερκαλιαιμική μεταβολική οξέωση εμφανίζεται στο 25-40% των ασθενών10. Όσο πιο κεντρικά είναι το τμήμα του γαστερεντερικού σωλήνα που χρησιμοποιείται τόσο πιο πιθανές να εμφανισθούν οι παραπάνω διαταραχές. Αν ο ειλεός χρησιμοποιείται για την ουρητηροστομία υπερχλωραμική μεταβολική οξέωση παρουσιάζεται έως στο 70% των ασθενών. Συστηματική οξέωση που να χρήζει θεραπείας παρατηρείται στο 10% της ομάδας αυτής των ασθενών , ενώ το 20% παρουσιάζει σποραδικά επεισόδια υπερχλωραιμικής μεταβολικής οξέωσης11. Όταν χρησιμοποιείται το κόλον 10-15% των ασθενών θα εμφανίσουν οξέωση. Μέχρι το 80% των ασθενών με ουρητηρο-σιγμοειδοστομία θα εμφανίσουν υπερχλωραιμική μεταβολική οξέωση, ενώ αν χρησιμοποιηθεί ειλεός ή κόλον η συχνότητα εμφάνισης των επεισοδίων κυμαίνεται μεταξύ 10-65%12. Τα ποσοστά αυτά είναι ψηλότερα αν η μέτρηση των αερίων αίματος και η αξιολόγηση του μεταβολικού προφίλ γίνει με προσοχή και σύστημα. Άλλες ηλεκτρολυτικές διαταραχές που έχουν περιγραφεί είναι υποκαλιαιμία, υπομαγνησιαιμία, υπασβεστιαιμία, υπεραμμωνιαιμία και βέβαια όπως έχει αναφερθεί επηρεασμένη νεφρική λειτουργία. Οι παραπάνω διαταραχές μπορεί να γίνουν πολύ σοβαρές όπως παράλυση λόγω υποκαλιαιμίας, νευρομυική δυσλειτουργία λόγω υπομαγνησιαιμίας και διαταραχές του οστικού μεταβολισμού λόγω των επιπέδων του ασβεστίου.
Παθοφυσιολογία
Για να γίνει αντιληπτή η παθοφυσιολογία των παραπάνω διαταραχών είναι απαραίτητο να γίνει κατανοητή η φιλοσοφία της μεταφοράς αλάτων και νερού μέσα από το εντερικό επιθήλιο. Η μεταφορά του νερού ακολουθεί το osmotic gradient και εξαρτάται από το tight-ness της μεμβράνης. Για παράδειγμα όταν χρησιμοποιείται το στομάχι παρά την οσμωτική διαφορά μεταξύ αίματος και εντερικού σωλήνα η μετακίνηση νερού είναι περιορισμένη. Αντίθετα το λεπτό έντερο είναι πιο «χαλαρή» μεμβράνη και γρήγορη εξισορρόπηση της συγκέντρωσης του νερού εκατέρωθεν της εντερικής μεμβράνης παρατηρείται ακολουθώντας τους κανόνες της οσμωτικής διαφοράς. Με αυτόν τον τρόπο οι ασθενείς αυτοί χάνουν μεγάλες ποσότητες ύδατος. Ο ειλεός είναι ελαφρώς καλύτερος από το λεπτό έντερο στο να διατηρεί την οσμωτική διαφορά εκατέρωθεν της μεμβράνης γιατί οι συνδέσεις μεταξύ των κυττάρων είναι πιο αποτελεσματικές. Το κόλον είναι το πιο αποτελεσματικό τμήμα του εντέρου στο να διατηρεί την οσμωτική διαφορά μεταξύ εντερικού σωλήνα και αιματικής ροής. Για το λόγο αυτό οι ασθενείς με ουρητηροστομία στον ειλεό χάνουν νερό ιδιαίτερα όταν τα ούρα παραμείνουν σε επαφή με τον εντερικό βλεννογόνο για μεγάλο διάστημα. Το φαινόμενο αυτό είναι λιγότερο συχνό όταν χρησιμοποιείται το κόλον, εμφανίζεται όμως όταν το εντερικό επιθήλιο παραμείνει σε επαφή με ούρα για μεγάλο διάστημα11.
H πλειοψηφία των ηλεκτρολυτών διαπερνούν το εντερικό τoίχωμα διασχίζοντας το εντερικό επιθήλιο. Ωστόσο παρατηρείται κάποια δραστηριότητα και μεταξύ των κυττάρων, όπου οι ηλεκτρολύτες μετακινούνται κατά ζεύγη. Είτε κινούνται προς την ίδια είτε σε αντίθετη κατεύθυνση έτσι όταν εκκρίνεται ένα ιόν απορροφάται ένα άλλο. Υπάρχει η γνωστή αντλία Na+/K+ η οποία επηρεάζει την συγκέντρωση του ενδοκυττάριου Na+ και έμμεσα επηρεάζει το ενδοκυττάριο p H. Αυτή η αντλία επηρεάζει την μετακίνηση ιόντων στην αυλική επιφάνεια της μεμβράνης, αλλάζοντας την ενδοκυττάρια συγκέντρωση ιόντων επηρεάζοντας με αυτόν τον τρόπο την κλίση (gradient) από τον αυλό στο κύτταρο. Στα όρια του αυλού υπάρχει ένας sodiumhydrogenexchanger και ένας bicarbonate-chlorideexchanger. Σύμφωνα με αυτήν την διαδικασία στον αυλό του εντέρου, το ιόν του υδρογόνου (Η+) εκκρίνεται ως αντάλλαγμα του νατρίου (Na+) και τα διττανθρακικά (HCO3-) ως αντάλλαγμα του χλωρίου (Cl-). Η παραπάνω διαδικασία κάτω από ορισμένες συνθήκες μπορεί να αναστραφεί. Na+, Cl-, Κ+, απορροφώνται και μέσω άλλων μηχανισμών. Πιστεύεται ότι ο κύριος όγκος του καλίου μετακινείται από τον αυλό στο αίμα παθητικά. Δεδομένου ότι τα ούρα έχουν γενικά υψηλές συγκεντρώσεις αμμωνίας (ΝΗ3), αμμωνίου (ΝΗ4+), υδρογόνου και χλωρίου, οι ουσίες αυτές επαναρροφώνται στα τμήματα του εντέρου που εκτίθεται σε ούρα. Πιστεύεται μάλιστα ότι η ιονισμένη μορφή της αμμωνίας μεταφέρεται μέσω των καναλιών Κ+ ή ότι διευκολύνεται από την από το sodiumhydrogenexchanger. Μία σειρά από διαλυμένες ουσίες μετακινούνται σύμφωνα με την κλίση συγκέντρωσης (gradient). Αυτό αφορά ιδιαίτερα το κάλιο, την αμμωνία, την κρεατινίνη και την ουρία. Η παθητική μετακίνηση ουρίας και κρεατινίνης κατά μήκος του εντερικού αυλού καθιστά την εκτίμηση της νεφρικής λειτουργίας σε ασθενείς με ουρητηρο-στομίες ιδιαίτερα δύσκολη. Για να περιορίσεις την παθητική μετακίνηση αυτών των ουσιών είναι απαραίτητο να διατηρείται μία διούρηση 150-250 ml την ώρα και να υπολογίζεται η κάθαρση κρεατινίνης με μεγαλύτερη ακρίβεια.
Αφού το νερό μετακινείται με βάση την osmotic gradient, μεγάλες απώλειες υγρών με συνοδό κίνδυνο αφυδάτωσης μπορεί να παρατηρηθεί σε ασθενείς όπου τμήμα του εντέρου έχει εκτεθεί στην ουροφόρο οδό. Παρατηρείται γρήγορη μετακίνηση νερού στην νήστιδα, λιγότερη έντονη στον ειλεό και ακόμα λιγότερη στο κόλον. Η μικρότερη μετακίνηση νερού παρατηρείται στο στομάχι. Παρόλα αυτά αν τα ούρα παραμείνουν σε επαφή με τμήμα του εντέρου για μεγάλο χρονικό διάστημα, μεγάλες απώλειες νερού παρατηρούνται ακόμα και αν το τμήμα του εντέρου είναι το κόλον. Αυτοί οι ασθενείς μπορεί να έχουν διούρηση 3000-4500 ml την ημέρα, η οποία ευθύνεται για την νυχτερινή ακράτεια.
Μηχανισμός βλάβης
Η κύρια διαταραχή που εμφανίζεται όταν ειλεός ή κόλον χρησιμοποιείται για την στομία είναι υπερχλωραιμική μεταβολική οξέωση (Σχ. 1). Έχει δειχθεί ότι τα τμήματα αυτά του εντέρου εκκρίνουν νάτριο και διττανθρακικά και επαναρροφούν αμμωνία, ιόντα υδρογόνου και χλωρίου. Στον τελικό ειλεό η επαναρρόφηση καλίου είναι μεγαλύτερη από ότι στο κόλον. Μελέτες έχουν δείξει ότι Na+ εκκρίνεται ως αντάλλαγμα του Η+ και τα HCO3- ως αντάλλαγμα του Cl-. Το κύριο ζευγάρι συμμετοχής στον μηχανισμό της οξέωσης είναι το πρώτο. Επίσης φαίνεται ότι η μεταφορά αμμώνιου προμηθεύει τον οργανισμό με περίσσεια πρωτονίων η οποία συνεχίζεται παρά την μη ευνοική κλίση συγκέντρωσης. Λόγω της υψηλής σταθεράς διαστάσεως (pKα 9,03) πολύ μικρή ποσότητα αμμωνίου ανιχνεύεται σε μη ιονισμένη μορφή στο p H που δημιουργείται όταν ούρα περάσουν μέσα από τμήμα του εντέρου. Παρά το γεγονός αυτό η συγκέντρωση της ολικής αμμωνίας στον αυλό συνεχώς ελαττώνεται. Στην ουσία του μηχανισμού, το ΝΗ4+ παράγει πρωτόνια (Η+) τα οποία μεταφέρονται στο κύτταρο σε ανταλλαγή του Na+, ή υποκαθιστά το Κ+ στον μεταφορέα 2CI-/K+/Na+. Mε τον παραπάνω μηχανισμό αυξάνεται το p H στο περιβάλλον της μεμβράνης του αυλού, γεγονός που με την σειρά του οδηγεί σε αύξηση της συγκέντρωσης της NH3, ευνοώντας την διάχυση της στο κύτταρο όπου και αποκτά το πρωτόνιο13 (Σχ. 2). Το φαινόμενο αυτό οδηγεί σε μετατόπιση του ΝΗ4+ στο εσωτερικό του κυττάρου. Παράλληλα το ΝΗ4+ αντικαθιστά το Κ+ και έτσι μεταφέρεται στο εσωτερικό του κυττάρου στη ιονισμένη του μορφή. Η μεταφορά αυτή εξισορροπείται από την απορρόφηση του Cl- επιτυγχάνοντας με αυτόν τον τρόπο ηλεκτρική ουδετερότητα εκατέρωθεν της μεμβράνης. Αξίζει να σημειωθεί ότι το ΝΗ4+ και το Κ+ έχουν ως ιόντα την ίδια ακτίνα και έχει δειχθεί ότι η μεταφορά τους μέσα από τμήματα εντέρου έχει ευθεία συσχέτιση όταν οι ροές νατρίου και καλίου συγκρίνονται με την επαναρρόφηση του αμμωνίου, δείχνοντας με αυτόν τον τρόπο ότι το ΝΗ4+ αναπληρώνει το Κ+ (Σχ. 3). Το ίδιο ακριβώς φαινόμενο παρατηρείται στο παχύ ανιόν σκέλος της αγκύλης του Henle. Προκύπτει έτσι από τα παραπάνω ότι η μεταφορά της ιονισμένης μορφής αμμωνίας μέσα από τμήμα του εντέρου έχει σημαίνοντα ρόλο στην εμφάνιση της οξέωσης. Το φαινόμενο έχει παρατηρηθεί και πειραματικά όταν προστέθηκε ουρεάση (που οδηγεί στην παραγωγή αμμωνίας από ουρία) σε περιβάλλον εντερικού αυλού11.
Σχήμα 1: Ένα από τα αίτια υπερχλωραιμικής μεταβολικής οξέωσης είναι η διενέργεια ουρητηροστομίας.

(Το σχήμα προέρχεται από Άτλαντα Νεφρολογίας του Shrier)
Σχήμα 2. Προτεινόμενος μηχανισμός υπερχλωραιμικής μεταβολικής οξέωσης, η οποία εμφανίζεται όταν δημιουργούνται ουρητηροστομίες στον ειλεό ή στο κόλον.
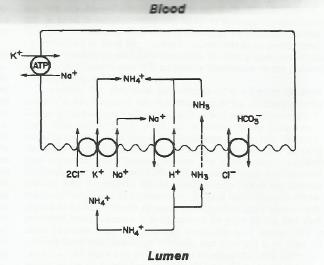
(Το σχήμα προέρχεται από το άρθρο του McDougal WS. Metabolite complications of urinary intestinal diversion. J Urol 1992;147:1199-1208.)
Σχήμα 3. Oι ροές νατρίου και καλίου συγκρίνονται με την επαναρρόφηση του αμμωνίου, δείχνοντας με αυτόν τον τρόπο ότι το ΝΗ4+ αναπληρώνει το Κ+.
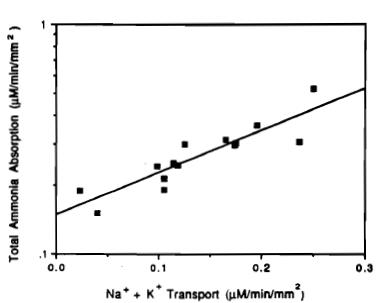
(Το σχήμα προέρχεται από το άρθρο του McDougal WS. Metabolite complications of urinary intestinal diversion. J Urol 1992;147:1199-1208.)
Θεραπεία
Η θεραπεία της υπερχλωραιμκής μεταβολικής οξέωσης περιλαμβάνει χορήγηση αλκαλιωτικών παραγόντων και/ή αναστολέων της μεταφοράς Cl-. Η χορήγηση από του στόματος διττανθρακικών μπορεί να αναπληρώσει το έλλειμμα στην οξεοβασική ισορροπία, από κάποιους ασθενείς όμως δεν γίνεται εύκολα ανεκτή. Σε αυτούς τους ασθενείς όπου παρατηρείται εμμένουσα υπερχλωραιμική μεταβολική οξέωση και η φόρτωση με παραπάνω νάτριο είναι ανεπιθύμητη μπορεί να χρησιμοποιηθεί χλωροπρομαζίνη ή νικοτινικό οξύ για να περιορισθεί ο βαθμός της οξέωσης. Τόσο η χλωροπρομαζίνη όσο και το νικοτινικό οξύ αναστέλλουν τη δράση της cyclic adenosine monophosphate και έτσι εμποδίζουν τη μεταφορά Cl-.
Mε το σκεπτικό ότι ο πιθανός μηχανισμός της υπερχλωραιμικής μεταβολικής οξέωσης βασίζεται στην επαναρρόφηση αμμωνίου, φαίνεται λογικό η θεραπεία της να βασίζεται στον περιορισμό του παραπάνω φαινομένου. Αφού το ΝΗ4+ προμηθεύει ένα Η+ και ταυτόχρονα ανταγωνίζεται με το Κ+ στο ίδιο κανάλι μεταφοράς μοιάζει λογικό οι αυξημένες συγκεντρώσεις νατρίου και καλίου να εμποδίζουν την επαναρρόφηση ΝΗ4+. Οι ασθενείς αυτοί επομένως μπορούν να λαμβάνουν κιτρικό νάτριο και κάλιο εφόσον διατηρούν φυσιολογική νεφρική λειτουργία, είτε σε χρόνια βάση στη λογική της προφύλαξης είτε επιθετικά για αποκατάσταση μίας σοβαρής οξέωσης. Αν οι ασθενείς έχουν καρδιολογικό ή νεφρολογικό ιστορικό που εμποδίζει την ευρεία χρήση των παραπάνω παραγώγων, ο συνδυασμός τους με χλωροπρομαζίνη ή νικοτινικό οξύ θα μπορούσε να αποβεί χρήσιμος θεραπευτικά 11,12.
Ηλεκτρολυτικές διαταραχές
Υποκαλιαιμία.
Οι ασθενείς με εκτροπή των ούρων παρουσιάζουν ελαττωμένες αποθήκες καλίου λόγω εντερικών απωλειών, ωσμωτικής διούρησης και νεφρικής έκκρισης.
Πιο έντονο είναι το φαινόμενο στους ασθενείς με ουρητηροσιγμοειδοστομία. Σε μελέτη ασθενών με ουρητηρο-κολονο-στομία παρατηρήθηκε ελάττωση των αποθηκών καλίου μέχρι και 30%, γεγονός που δεν παρατηρήθηκε τόσο έντονο σε ασθενείς όπου χρησιμοποιήθηκε ο τελικός ειλεός (14%). Έχει δειχθεί ότι όταν τμήματα του ειλεού έρθουν σε επαφή με ούρα επαναρροφούν μεγάλο τμήμα του καλίου που περιέχεται σε αυτά, ενώ στο κόλον το φαινόμενο δεν είναι τόσο έντονο. Θα πρέπει να έχουμε κατά νου ότι η θεραπεία της μεταβολικής οξέωσης, επιτείνει την υποκαλιαιμία. Κλινικά, αυτό μπορεί να γίνει εμφανές με μυϊκή αδυναμία του ασθενούς.
Έχουν αναφερθεί περιπτώσεις ασθενών με γενικευμένη μυϊκή αδυναμία, η οποία έχει αποδοθεί σε σύνδρομο Guillain-Barré, ενώ οφείλεται σε υποκαλιαιμία μετά από ουρητηρο-εντερο στομία 14,15,16. Ως εκ τούτου, δεν πρέπει να ξεχνάμε τη χρήση συμπληρωμάτων καλίου κατά τη διόρθωση της οξέωσης σε ασθενείς μετά από εκτροπή των ούρων17.
Υπασβεστιαιμία / υπομαγνησιαιμία
Η χρόνια μεταβολική οξέωση σε ασθενείς με εκτροπή των ούρων ρυθμίζεται από τα ανθρακικά άλατα των οστών. Αυτό έχει ως αποτέλεσμα συνεχή απελευθέρωση ασβεστίου από τα οστά. Αυτή η περίσσεια του ασβεστίου του ορού απεκκρίνεται από τα νεφρά, όπου η παρουσία της οξέωσης περαιτέρω αναστέλλει την επαναρρόφηση του ασβεστίου 18. Κλινικά σημαντική υπασβεστιαιμία δεν είναι συχνή. Συμπληρώματα ασβεστίου είναι η θεραπεία εκλογής.
Η υπομαγνησιαιμία είναι μια σπάνια κατάσταση μετά από ουρητηρο-εντερο στομία. Το διατροφικό έλλειμμα παίζει σημαντικό ρόλο μαζί με συνοδές νεφρικές απώλειες, αφού η νεφρική σωληναριακή επαναρρόφηση μαγνησίου επηρεάζεται από την διαταραχή του μεταβολισμού του ασβεστίου και την συνυπάρχουσα οξέωση 18.
Συμπτώματα προκαλούνται όταν τα επίπεδα μαγνησίου πέσουν κάτω από 1 mEq/L . Σε αυτές τις περιπτώσεις η κλινική εικόνα περιλαμβάνει νευρομυικές διαταραχές, διαταραχή της προσωπικότητας απλές ή και πιο σοβαρές, τρόμο και σπάνια τετανία. Σε ακραίες καταστάσεις ελλείμματος που δεν διορθώνεται μπορεί να εμφανισθούν σπασμοί και θάνατος.
Λιθίαση
Η υπερχλωραιμική μεταβολική οξέωση οδηγεί σε αυξημένη νεφρική απέκκριση ασβεστίου και ιόντων υδρογόνου και συνδέεται συχνά με υποκιτρικουρία. Η δυσαπορρόφηση του λίπους που μπορεί να παρατηρηθεί σε αυτήν την ομάδα των ασθενών μπορεί να προκαλέσει υπεροξαλουρία. Τα παραπάνω φαινόμενα οδηγούν στην δημιουργία λίθων (calcium phosphate and/or calcium oxalate). Η τάση των ασθενών να εμφανίζουν αφυδάτωση αυξάνει περαιτέρω την προδιάθεση για σχηματισμό λίθων. Ο χρόνιος αποικισμός/λοίμωξη της ουροφόρου οδού , ειδικά με βακτήρια που παράγουν ουρεάση, θα οδηγήσει με τη σειρά του επίσης στον σχηματισμό λίθων (struvite and/or carbonate apatite). Μετά από 20 χρόνια παρακολούθησης, έως και 20% των ασθενών με ουρητηρο-εντερο στομία θα έχουν νεφρολιθίαση 19. Στην τακτική παρακολούθηση των ασθενών με εκτροπή των ούρων, πρέπει να περιλαμβάνεται η υπερηχογραφική απεικόνιση των νεφρών για τον έλεγχο σχηματισμού λίθων. Προδιαθεσικοί παράγοντες για τον σχηματισμό λίθων είναι η παρουσία ξένων υλικών (όπως ράμματα), η εντερική βλέννα και η παρουσία υπολειμματικών ούρων.
Οστική νόσος
Θεωρητικά, μία βασική επιπλοκή της εκτροπής των ούρων είναι η αφαλάτωση των οστών. Η χρόνια υπερχλωραιμική μεταβολική οξέωση (η οποία σε διαφορετικό βαθμό εμφανίζεται στην πλειοψηφία της ομάδας αυτής των ασθενών), ρυθμίζεται από τα ανθρακικά άλατα των οστών. Η κινητοποίηση, ασβεστίου, ανθρακικών αλάτων και νατρίου οδηγεί στην αφαλάτωση. Παράλληλα, η οξέωση επηρεάζει την ενεργοποίηση (νεφρική συνιστώσα) της βιταμίνης D και ενεργοποιεί τους οστεοκλάστες, που προάγουν με τη σειρά τους την οστική απορρόφηση. Λόγω της χρήσης τμήματος εντέρου για την εκτροπή των ούρων επηρεάζεται επίσης η εντερική απορρόφηση ασβεστίου και βιταμίνης D. Φαίνεται ότι σε αυτήν τη ομάδα των ασθενών το γινόμενο ασβεστίου-φωσφώρου είναι ελαττωμένο σε σχέση με τον υγιή πληθυσμό και η νεφρική απέκκριση ασβεστίου, όπως αναφέρθηκε στον μηχανισμό σχηματισμού λίθων, είναι αυξημένη. Φαίνεται επίσης ότι η αυξημένη αυτή απέκκριση είναι αποτέλεσμα ελαττωμένης σωληναριακής επαναρρόφησης ασβεστίου. Σε αυτήν την αλληλουχία των γεγονότων η παραθορμόνη δεν έχει σημαίνοντα ρόλο (η τιμή της στους ασθενείς με φυσιολογική νεφρική λειτουργία είναι εντός των ορίων). Ο ρόλος της καλσιτονίνης δεν έχει μελετηθεί και είναι άγνωστος 1.11.
Στην κλινική πράξη, σε σειρές ασθενών με ουρητηρο-εντερο-στομίες σοβαρές μεταβολικές διαταραχές των οστών που να έχουν οδηγήσει σε οστεομαλακία δεν έχουν παρατηρηθεί. Το πιό πιθανό είναι να παρατηρηθούν μικρές διαταραχές της αφαλάτωσης των οστών στην πλειοψηφία των ασθενών που έχουν ουρητηρο-εντερο-στομίες για μέγαλη χρονική περίοδο. Έχει φανεί ότι σε σειρά ασθενών με τέτοιου τύπου εκτροπή των ούρων για διάστημα 17-23 ετών οι ασθενείς εμφάνισαν αυξημένο αριθμό καταγμάτων ή άλλων ορθοπεδικών προβλημάτων χωρίς να είναι ιδαίτερα οξεωτικοί κατά τη διάρκεια της παρακολούθησης. Ωστόσο, ασθενείς με επηρεασμένη νεφρική λειτουργία, γυναίκες ιδιαίτερα της μετεμμηνοπαυσιακής ηλικίας, παιδιά, είναι ομάδες αυξημένου κινδύνου για διαταραχές του οστικού μεταβολισμού. Ασθενείς με την κλινική οντότητα παραπονιούνται για πόνο, ενώ από τον εργαστηριακό τους έλεγχο έχουν φυσιολογικά ή ελαττωμένα επίπεδα ασβεστίου και φωσφώρου και συνήθως αυξημένα επίπεδα αλκαλικής φωσφατάσης.
Δεν υπάρχει σαφής οδηγία σχετικά με τα μέτρα παρακολούθησης και πρόληψης που θα πρέπει να λαμβάνονται, ιδιαίτερα στις ομάδες αυξημένου κινδύνου. Φαίνεται ότι σε αυτήν την ομάδα των ασθενών η παρακολούθηση για τον έλεγχο οστεοπόρωσης είναι απαραίτητη. Ασυμπτωματικοί ασθενείς με φυσιολογική νεφρική λειτουργία μάλλον δεν χρειάζονται ιδιαίτερη παρακολούθηση της οστικής τους πυκνότητας. Θεραπεία της μεταβολικής οξέωσης με αλκαλωτικούς παράγοντες και βιταμίνη C είναι επαρκή μέτρα προφύλαξης. Σε πιο σοβαρές περιπτώσεις, χορήγηση βιταμίνης D και ασβεστίου κρίνονται απαραίτητα 1,11.
Mεταμόσχευση παγκρέατος
Για να αποκτήσει ένας ασθενής νησίδια παγκρέατος ικανά να παράγουν ινσουλίνη και να θεραπεύσουν τον σακχαρώδη διαβήτη είναι απαραίτητη η μεταμόσχευση τόσο της εξωκρινούς όσο και της ενδοκρινούς μοίρας του παγκρέατος. Αυτή η πραγματικότητα θα αλλάξει όταν η εμφύτευση νησιδίων του παγκρέατος γίνει μία διαθέσιμη και αξιόπιστη επιλογή. Στην παρούσα φάση τρεις δυνατότητες υπάρχουν: α) μεμονωμένη μεταμόσχευση παγκρέατος, β) συνδυασμένη μεταμόσχευση νεφρού-παγκρέατος και γ) μεταμόσχευση παγκρέατος σε ασθενή με ήδη επιτυχημένη μεταμόσχευση νεφρού. Κάθε μία από τις παραπάνω καταστάσεις χαρακτηρίζεται από πλεονεκτήματα και μειονεκτήματα.
Ο αριθμός των ασθενών που υποβάλλονται σε μεμονωμένη μεταμόσχευση παγκρέατος αυξάνεται τα τελευταία χρόνια. Παρόλα αυτά η νορμογλυκαιμία που επιτυγχάνεται μετά από μία τέτοια επιτυχημένη επέμβαση δεν εξασφαλίζει την υποστροφή της διαβητικής νεφροπάθειας και/ή αμφιβληστροειδοπάθειας. Παράλληλα ο ασθενής εκτείθεται σε μία χειρουργική επέμβαση και λαμβάνει επί μακρόν ανοσοκατασταλτική αγωγή. Στην μεταμόσχευση παγκρέατος σε ασθενή με ήδη επιτυχημένη μεταμόσχευση νεφρού, δυστυχώς οι δευτεροπαθείς επιπλοκές του διαβήτη είναι σε μεγάλο βαθμό εγκατεστημένες. Στην περίπτωση αυτή το όφελος της επέμβασης περιορίζεται στην ανεξαρτησία που προσφέρεται στον ασθενή σε σχέση με τη χρήση ινσουλίνης. H συνδυασμένη μεταμόσχευση νεφρού-παγκρέατος θεωρείται ο καλύτερος τύπος μεταμόσχευσης παγκρέατος. Πρόκειται για μία χειρουργική επέμβαση μεταμόσχευσης δύο οργάνων και η ανοσοκατασταλτική αγωγή είναι παρόμοια με αυτήν της μεμονωμένης μεταμόσχευσης νεφρού. Όπως και στην μεμονωμένη μεταμόσχευση παγκρέατος δυστυχώς και στην περίπτωση αυτή οι δευτεροπαθείς επιπλοκές του διαβήτη είναι σε μεγάλο βαθμό εγκατεστημένες και ο βαθμός σταθεροποίησης τους ή και υποστροφής τους παραμένει αβέβαιος24.
Πολλή συζήτηση γίνεται για τη διαχείρηση των εκκρίσεων της εξωκρινούς μοίρας του παγκρέατος μετά την μεταμόσχευση. Οι πιο κοινές τεχνικές είναι η παροχέτευση μέσω εντέρου (Σχ.4) ή μέσω ουροδόχου κύστεως (Σχ. 5). Η πρώτη είναι και η πιο δημοφιλής. Σε αυτήν την περίπτωση όλο το πάγκρεας μαζί με ένα τμήμα του δωδεκαδακτύλου του δότη μεταμοσχεύεται σε πλαγιο-πλάγια αναστόμωση με τμήμα του λεπτού εντέρου. Με αυτόν τον τρόπο αποφεύγονται οι ουρολοιμώξεις, τα επεισόδια παγκρεατίτιδας και το μεταβολικό προφίλ του ασθενούς είναι καλύτερο. Το μεγαλύτερο πρόβλημα σε αυτήν την τεχνική είναι εμφάνιση διαρροής από τη αναστόμωση που μπορεί να οδηγήσει σε απώλεια του μοσχεύματος και σήψη και η αδυναμία μέτρησης της αμυλάσης ούρων για πιθανή απόρριψη25.
Όλο και λιγότερα κέντρα επιλέγουν την παροχέτευση των εκκρίσεων της εξωκρινούς μοίρας του παγκρέατος στην ουροδόχο κύστη. Τα πλεονεκτήματα της μεθόδου είναι λιγότερες χειρουργικές επιπλοκές. Δεν είναι λίγα όμως και τα μειονεκτήματα. Παρατηρείται σημαντική απώλεια διττανθρακικών ενώ και τα επεισόδια των ουρολοιμώξεων είναι πιο συχνά.
Σχήμα 4: Παροχέτευση μέσω εντέρου.
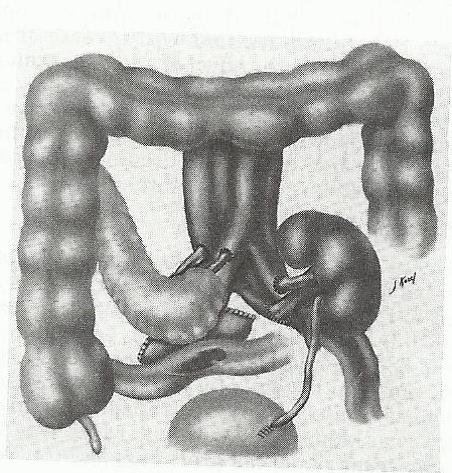
Η εικόνα προέρχεται από

Σχήμα 5: Παροχέτευση μέσω ουροδόχου κύστεως.
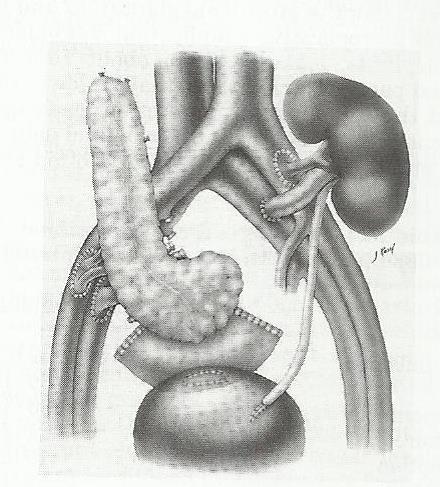
Η εικόνα προέρχεται από

Ουρολοιμώξεις
Αποτελούν συχνό φαινόμενο. Συχνό αίτιο για επίμονες ουρολοιμώξεις είναι παραμονή των ραμμάτων στην αναστόμωση και τα οποία κανονικά αφαιρούνται κυστεοσκοπικά. Η παραμονή τους προδιαθέτει στον σχηματισμό λίθων. Είναι αποτέλεσμα της αλλαγής του φυσιολογικού περιβάλλοντος της κύστεως λόγω των εκκρίσεων της εξωκρινούς μοίρας του παγκρέατος. Αν το φαινόμενο παραμένει κρίνεται απαραίτητη η δημιουργία εντερικής παράκαμψης26.
Αιματουρία
Συνήθως εμφανίζεται στην άμεση μετεγχειρητική περίοδο από αγγείο που αιμορραγεί είτε στην περιοχή των ραμμάτων είτε στο τμήμα του δωδεκαδακτύλου. Η χρόνια αιματουρία μπορεί να οφείλεται είτε σε έλκος στο τμήμα του δωδεκαδακτύλου, είτε σε ινώδη ιστό ή τέλος σε εμμένουσα κυστίτιδα. Στην οξεία φάση με κυστεοσκόπηση απομακρύνεται ο θρόμβος και καυτηριάζεται το σημείο αιμορραγίας. Σε χρόνιες περιπτώσεις απομακρύνονται τα ράμματα, εξαιρείται ο ινώδης ιστός ή τέλος ακολουθείται η οδός της εντερικής παράκαμψης26.
Μεταβολικές διαταραχές
Το βασικό αίτιο των μεταβολικών διαταραχών σε αυτούς τους ασθενείς η απώλεια μεγάλων ποσοτήτων παγκρεατικού υγρού πλούσιου σε αλκαλικά ένζυμα μέσω της ουροφόρου οδού. Μεταβολική οξέωση, υπονατριαιμία και απώλεια υγρών από τον εξωκυττάριο χώρο μπορεί να παρατηρηθούν. Η αντιμετώπιση τους συνιστά την χορήγηση είτε από το στόμα είτε σε πιο σοβαρές καταστάσεις ενδοφλέβια, άλατος καθώς και διττανθρακικών. Σε ασθενείς που λαμβάνουν tacrolimus τα διττανθρακικά πρέπει να χορηγούνται 2 ώρες πριν ή μετά από τη λήψη του φαρμάκου για να μην παρεμποδίζεται η απορρόφηση του27.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Van der Aa F, De Ridder D, Van Poppel H. Van der Aa F. When the Bowel Becomes the Bladder: Changes in metabolism after urinary diversion. Nutrition issues in Gastrenterology 2012;107:15-28.
- Bricker, E.M., Bladder substitution after pelvic evisceration. Surg Clin North Am, 1950. 30(5):1511-21.
- Hautmann, R.E., K. Miller, U. Steineret al., The ileal neoblad¬der: 6 years of experience with more than 200 patients. J Urol, 1993;150(1):40-5.
- Hautmann, R.E., Surgery illustrated - surgical atlas ileal neo¬bladder. BJU Int. 105(7):1024-35.
- Studer, U.E., C. Varol and H. Danuser, Orthotopic ileal neoblad¬der. BJU Int, 2004; 93(1):183-93.
- Joniau, S., J. Benijts, M. Van Kampenet al., Clinical experience with the N-shaped ileal neobladder: assessment of complica¬tions, voiding patterns, and quality of life in our series of 58 patients. Eur Urol, 2005;47(5):666-72; discussion 72-3.
- Ghoneim, M.A., A.A. Shaaban, M.R. Mahranet al., Further expe¬rience with the urethral Kock pouch. J Urol, 1992;147(2):361-5.
- Bakke, A., K.M. Jensen, O. Jonssonet al., The rationale behind recommendations for follow-up after urinary diver¬sion: an evidence-based approach. Scand J Urol Nephrol, 2007;41(4):261- 9.
- Kristjansson, A., L. Wallin and W. Mansson, Renal function up to 16 years after conduit (refluxing or anti-reflux anastomosis) or continent urinary diversion. 1. Glomerular filtration rate and patency of uretero-intestinal anastomosis. Br J Urol, 1995;76(5):539-45.
- Klein E, Montie JE, Montague DK, et al. Jejunal conduit urinary diversion. J Urol 1986;135:244.
- McDougal WS. Metabolite complications of urinary intestinal diversion. J Urol 1992;147:1199-1208.
- Silverman SH, Woodhouse CR, Strachan JR, et al. Long term management of patients who have had urinary diversions into colon. Br J Urol 1986;58:634-639.
- Valtier, B., G. Mion, L.H. Phamet al., Severe hypokalaemic paralysis from an unusual cause mimicking the Guillain-Barre syndrome. Intensive Care Med, 1989;15(8):534-5.
- Van Bekkum, J.W., D.J. Bac, I.E. Nienhuiset al., Life-threatening hypokalaemia and quadriparesis in a patient with ureterosig¬moidostomy. Neth J Med, 2002. 60(1):26-8.
- Rafique, M., Life threatening hypokalemia and quadriparesis in a patient with ureterosigmoidostomy. Int Urol Nephrol, 2006;38(3-4):453-6.
- Koch M,O, McDougal WS, Thompson CO. Mechanisms of solute transport following urinary diversion through interstinal segments: an experimental study with rats. J. Urol 1991;146:1390.
- Koff, S.A., Mechanism of electrolyte imbalance following uro¬intestinal anastomosis. Urology, 1975. 5(1):109-14.
- McDougal, W.S. and M.O. Koch, Effect of sulfate on cal¬cium and magnesium homeostasis following urinary diversion. Kidney Int, 1989;35(1):105-15.
- McDougal, W.A.K., M.O., Impaired growth and development and urinary intestinal interposition. Abst. Am. Assoc. GU Surg., 1991;105:3.
- Holmes, D.G., J.B. Thrasher, G.Y. Parket al., Long-term com¬plications related to the modified Indiana pouch. Urology, 2002;60(4):603-6.
- Skinner, D.G., G. Lieskovsky and S.D. Boyd, Continuing expe¬rience with the continent ileal reservoir (Kock pouch) as an alternative to cutaneous urinary diversion: an update after 250 cases. J Urol, 1987;137(6):1140-5.
- Terai, A., T. Ueda, Y. Kakehiet al., Urinary calculi as a late com¬plication of the Indiana continent urinary diversion: comparison with the Kock pouch procedure. J Urol, 1996;155(1):66-8.
- Hering BJ, Ricordi C. Islet transplantation for patients with type I diabetes. Graft 1999;2:12.
- Hricik DE. Combined kidney-pancreas transplantation. Kidney Int 1998;53:1091.
- Lederes E. Pancreas transplants for diabetic nephropathy: a time for reassessment. Amer J Kidney Dis 2000;35:1238.
- Stratta RJ. Review of immunosuppressive usage in pancreas transplantation. Clin Transplant 1999;13:1.
Σχετικά Άρθρα

Χρόνια Νεφρική Νόσος & Οξέωση

Αιμοκάθαρση και Φώσφορος (Δίαιτα, Δεσμευτικά, Κάθαρση)